FISICA NUCLEAR
OBJETIVO. Entender los conceptos de número atómico y número másico y emplearlos
para identificar átomos y representar iones.
Números atómico y másico
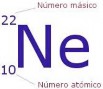 La identidad de un átomo y sus propiedades vienen dadas por el número de partículas que contiene. Lo que distingue a unos elementos químicos de otros es el número de protones que tienen sus átomos en el núcleo. Este número se llama Número atómico y se representa con la letra Z. Se coloca como subíndice a la izquierda del símbolo del elemento correspondiente.
La identidad de un átomo y sus propiedades vienen dadas por el número de partículas que contiene. Lo que distingue a unos elementos químicos de otros es el número de protones que tienen sus átomos en el núcleo. Este número se llama Número atómico y se representa con la letra Z. Se coloca como subíndice a la izquierda del símbolo del elemento correspondiente.
El Número másico nos indica el número total de partículas que hay en el núcleo, es decir, la suma de protones y neutrones. Se representa con la letra A y se sitúa como superíndice a la izquierda del símbolo del elemento. Representa, aproximadamente, la masa del átomo medida en uma, ya que la de los electrones es tan pequeña que puede despreciarse.

El símbolo tiene número atómico Z = 1. Por tanto, quiere decir que ese átomo tiene 1 protón en el núcleo. Es Hidrógeno.
El símbolo tiene número másico A = 2. Por tanto, quiere decir que ese átomo tiene 2 partículas en el núcleo, entre protones y neutrones. Como Z = 1, tiene 1 protón y A – Z = 2 -1 = 1 neutrón.
Iones
 Un catión es un átomo con carga positiva. Se origina por pérdida de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga +1, esto indica que ha perdido un electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón, al ser positivo lo ha perdido y, por ello, tiene 0 electrones.
Un catión es un átomo con carga positiva. Se origina por pérdida de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga +1, esto indica que ha perdido un electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón, al ser positivo lo ha perdido y, por ello, tiene 0 electrones.
 Un anión es un átomo con carga negativa. Se origina por ganancia de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga -1, esto indica que ha ganado 1 electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón; al tener carga -1 ha ganado otro; por tanto, tiene 2 electrones.
Un anión es un átomo con carga negativa. Se origina por ganancia de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga -1, esto indica que ha ganado 1 electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón; al tener carga -1 ha ganado otro; por tanto, tiene 2 electrones.
ACTIVIDADES.
RADIACTIVIDAD
OBJETIVO. Conocer el fenómeno de la Radiactividad y sus aplicaciones.
La radiactividad es un fenómeno en el cual, los núcleos de átomos que no son estables (suelen ser aquellos que tienen un número de neutrones muy superior al de protones), emiten partículas y radiaciones de forma espontánea hasta que consiguen estabilizarse. Esto hace que los núcleos de un elemento se transformen en núcleos de otro elemento diferente. Estos núcleos de isótopos radiactivos se denominan radioisótopos. Las partículas y radiaciones que pueden ser emitidas son:
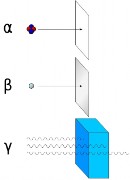
-Partículas alfa (α).
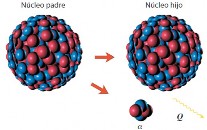 Cuando un núcleo padre de numero másico A y numero atómico Z emite una partícula alfa, se convierte en un nuevo núcleo, cuyo nuevo numero másico es (A–4), y su numero atómico queda como (Z–2). La transmutación queda descrita por la siguiente ecuación:
Cuando un núcleo padre de numero másico A y numero atómico Z emite una partícula alfa, se convierte en un nuevo núcleo, cuyo nuevo numero másico es (A–4), y su numero atómico queda como (Z–2). La transmutación queda descrita por la siguiente ecuación:
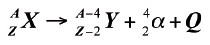
-Partículas beta (β).
Los experimentos han determinado que existen dos tipos de emisiones beta: la emisión β+, en que el núcleo emite un positrón (de carga positiva, pero con la masa del electrón), y la β-, en la que el núcleo emite un electrón.
a. Emisión beta positiva (β+)
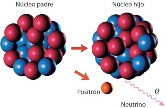 Lo que sucede en este tipo de emisión es que un protón del núcleo atómico pierde su carga eléctrica, es decir, se convierte en un neutrón. Generalmente, esto ocurre en núcleos cuya cantidad de protones es mayor que la de neutrones. En ese proceso, el protón emite un neutrino ν (con carga eléctrica nula y masa casi nula) y un positrón e+ (de carga eléctrica positiva y la misma masa que el electrón):
Lo que sucede en este tipo de emisión es que un protón del núcleo atómico pierde su carga eléctrica, es decir, se convierte en un neutrón. Generalmente, esto ocurre en núcleos cuya cantidad de protones es mayor que la de neutrones. En ese proceso, el protón emite un neutrino ν (con carga eléctrica nula y masa casi nula) y un positrón e+ (de carga eléctrica positiva y la misma masa que el electrón):
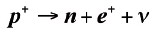
El proceso completo para el núcleo padre (X) y el núcleo hijo (Y) queda expresado en la siguiente ecuación:
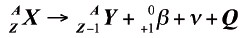
b. Emisión beta negativa (β-)
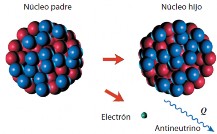 En este proceso, un neutrón del núcleo atómico experimenta un fenómeno en el cual se transforma en un protón, liberando un electrón. El protón permanece al interior del núcleo, mientras el electrón es expulsado. La partícula es un antineutrino, no tiene carga eléctrica y su masa es muy reducida. El proceso completo para el núcleo está representado por la siguiente ecuación:
En este proceso, un neutrón del núcleo atómico experimenta un fenómeno en el cual se transforma en un protón, liberando un electrón. El protón permanece al interior del núcleo, mientras el electrón es expulsado. La partícula es un antineutrino, no tiene carga eléctrica y su masa es muy reducida. El proceso completo para el núcleo está representado por la siguiente ecuación:
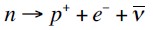
Recordemos que la energía Q se puede obtener de la ecuación de Einstein E = mc2, donde m será la diferencia entre la masa del núcleo antes y después de la emisión.
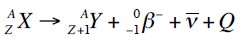
-Rayos gamma (γ).
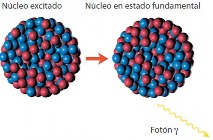 Luego de los procesos de decaimiento, generalmente los núcleos atómicos quedan excitados, es decir, en un estado energético mayor que el normal; entonces, para volver a su estado fundamental emiten una onda electromagnética de alta frecuencia: la radiación gamma. Lo anterior queda representado por la siguiente ecuación:
Luego de los procesos de decaimiento, generalmente los núcleos atómicos quedan excitados, es decir, en un estado energético mayor que el normal; entonces, para volver a su estado fundamental emiten una onda electromagnética de alta frecuencia: la radiación gamma. Lo anterior queda representado por la siguiente ecuación:
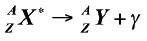
Donde el término 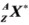 representa un núcleo excitado y γ, a uno o más fotones gamma. De acuerdo con el principio de cuantización de energía, la energía de los fotones emitidos corresponde a la energía de transición entre dos estados estacionarios. Los fotones gamma tienen niveles elevados de energía que varía de 1 Mev a 1 Gev, mientras que las longitudes de onda varía entre 0,1 y 0,01 nm.
representa un núcleo excitado y γ, a uno o más fotones gamma. De acuerdo con el principio de cuantización de energía, la energía de los fotones emitidos corresponde a la energía de transición entre dos estados estacionarios. Los fotones gamma tienen niveles elevados de energía que varía de 1 Mev a 1 Gev, mientras que las longitudes de onda varía entre 0,1 y 0,01 nm.
También puede haber emisión gamma cuando un núcleo es impactado por una partícula de masa elevada, dejándolo excitado; entonces, para volver a su estado fundamental emite uno o varios fotones gamma.
ACTIVIDADES.
DECAIMIENTO RADIACTIVO
OBJETIVO. Comprender cómo decaen las sustancias y su uso en la datación con C-14.
Como ya estudiamos, los núcleos inestables de los isotopos radiactivos tienden a buscar configuraciones más estables emitiendo radiaciones, proceso llamado desintegración o decaimiento radiactivo. Algunas características del decaimiento radiactivo son:
•
No es continuo, sino que se realiza en sucesivas emisiones.
•
Es aleatorio (no es posible predecir cual núcleo se desintegrara en un determinado instante).
•
Es posible determinar con gran precisión el número de átomos que decaerán en un intervalo de tiempo.
ACTIVIDADES.
FISIÓN NUCLEAR
OBJETIVO. Establecer la diferencia entre fusión y fisión nuclear, analizar las reacciones
que desencadena cada fenómeno y las aplicaciones actuales de cada una.
La fisión nuclear consiste en la rotura de núcleos de átomos "grandes" mediante bombardeo con neutrones, dando lugar a dos o más núcleos de átomos "pequeños" y algunas otras partículas. Además se libera gran cantidad de energía. El proceso comienza al bombardear el núcleo grande con partículas como neutrones. (Los neutrones son buenos proyectiles ya que al no tener carga son menos rechazados por parte del núcleo).
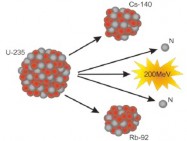 Además de núcleos de elementos con átomos más pequeños, se liberan otros neutrones que rompen otros núcleos grandes, en lo que se denomina una reacción en cadena.
Además de núcleos de elementos con átomos más pequeños, se liberan otros neutrones que rompen otros núcleos grandes, en lo que se denomina una reacción en cadena.
La gran cantidad de energía que se libera se llama energía nuclear. Esta energía se aprovecha en las centrales nucleares para obtener energía eléctrica. También es la responsable del efecto destructivo de las bombas atómicas y de los misiles nucleares.
Su reacción sucede de la manera que se presenta a continuación:
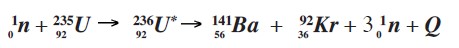
FUSIÓN NUCLEAR
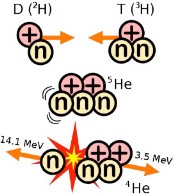 La fusión nuclear es un proceso en el que núcleos de átomos muy pequeños se unen para dar núcleos de átomos mayores. Dos átomos de hidrógeno pueden unir sus núcleos y convertirse en un átomo de helio. Este proceso se realiza continuamente en nuestro Sol y en todas las demás estrellas del Universo. Como resultado se desprende una gran cantidad de energía.
La fusión nuclear es un proceso en el que núcleos de átomos muy pequeños se unen para dar núcleos de átomos mayores. Dos átomos de hidrógeno pueden unir sus núcleos y convertirse en un átomo de helio. Este proceso se realiza continuamente en nuestro Sol y en todas las demás estrellas del Universo. Como resultado se desprende una gran cantidad de energía.
Esta fuente de energía tendría la gran ventaja de no producir residuos radiactivos. El problema es que lograr la fusión de forma controlada tiene grandes dificultades técnicas. Se requiere muchísima energía inicial (hay que poner los átomos de combustible a 100 millones de ºC) por eso esta reacción se denomina termonuclear. A esta temperatura la materia se encuentra en estado de plasma (átomos en un mar de electrones sueltos) y no se puede confinar en ningún recipiente porque ninguno soporta esta temperatura.
Su reacción sucede de la manera que se presenta a continuación:
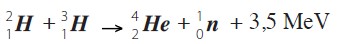
ACTIVIDADES.
ACTIVIDADES DE SELECCIÓN MÚLTIPLE
 La identidad de un átomo y sus propiedades vienen dadas por el número de partículas que contiene. Lo que distingue a unos elementos químicos de otros es el número de protones que tienen sus átomos en el núcleo. Este número se llama Número atómico y se representa con la letra Z. Se coloca como subíndice a la izquierda del símbolo del elemento correspondiente.
La identidad de un átomo y sus propiedades vienen dadas por el número de partículas que contiene. Lo que distingue a unos elementos químicos de otros es el número de protones que tienen sus átomos en el núcleo. Este número se llama Número atómico y se representa con la letra Z. Se coloca como subíndice a la izquierda del símbolo del elemento correspondiente. 
 Un catión es un átomo con carga positiva. Se origina por pérdida de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga +1, esto indica que ha perdido un electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón, al ser positivo lo ha perdido y, por ello, tiene 0 electrones.
Un catión es un átomo con carga positiva. Se origina por pérdida de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga +1, esto indica que ha perdido un electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón, al ser positivo lo ha perdido y, por ello, tiene 0 electrones.  Un anión es un átomo con carga negativa. Se origina por ganancia de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga -1, esto indica que ha ganado 1 electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón; al tener carga -1 ha ganado otro; por tanto, tiene 2 electrones.
Un anión es un átomo con carga negativa. Se origina por ganancia de electrones y se indica con un superíndice a la derecha. El símbolo de este átomo nos dice que tiene carga -1, esto indica que ha ganado 1 electrón. Este átomo tiene Z = 1, si fuera neutro tendría 1 electrón; al tener carga -1 ha ganado otro; por tanto, tiene 2 electrones. 
 Cuando un núcleo padre de numero másico A y numero atómico Z emite una partícula alfa, se convierte en un nuevo núcleo, cuyo nuevo numero másico es (A–4), y su numero atómico queda como (Z–2). La transmutación queda descrita por la siguiente ecuación:
Cuando un núcleo padre de numero másico A y numero atómico Z emite una partícula alfa, se convierte en un nuevo núcleo, cuyo nuevo numero másico es (A–4), y su numero atómico queda como (Z–2). La transmutación queda descrita por la siguiente ecuación:  Lo que sucede en este tipo de emisión es que un protón del núcleo atómico pierde su carga eléctrica, es decir, se convierte en un neutrón. Generalmente, esto ocurre en núcleos cuya cantidad de protones es mayor que la de neutrones. En ese proceso, el protón emite un neutrino ν (con carga eléctrica nula y masa casi nula) y un positrón e+ (de carga eléctrica positiva y la misma masa que el electrón):
Lo que sucede en este tipo de emisión es que un protón del núcleo atómico pierde su carga eléctrica, es decir, se convierte en un neutrón. Generalmente, esto ocurre en núcleos cuya cantidad de protones es mayor que la de neutrones. En ese proceso, el protón emite un neutrino ν (con carga eléctrica nula y masa casi nula) y un positrón e+ (de carga eléctrica positiva y la misma masa que el electrón):  En este proceso, un neutrón del núcleo atómico experimenta un fenómeno en el cual se transforma en un protón, liberando un electrón. El protón permanece al interior del núcleo, mientras el electrón es expulsado. La partícula es un antineutrino, no tiene carga eléctrica y su masa es muy reducida. El proceso completo para el núcleo está representado por la siguiente ecuación:
En este proceso, un neutrón del núcleo atómico experimenta un fenómeno en el cual se transforma en un protón, liberando un electrón. El protón permanece al interior del núcleo, mientras el electrón es expulsado. La partícula es un antineutrino, no tiene carga eléctrica y su masa es muy reducida. El proceso completo para el núcleo está representado por la siguiente ecuación:  Luego de los procesos de decaimiento, generalmente los núcleos atómicos quedan excitados, es decir, en un estado energético mayor que el normal; entonces, para volver a su estado fundamental emiten una onda electromagnética de alta frecuencia: la radiación gamma. Lo anterior queda representado por la siguiente ecuación:
Luego de los procesos de decaimiento, generalmente los núcleos atómicos quedan excitados, es decir, en un estado energético mayor que el normal; entonces, para volver a su estado fundamental emiten una onda electromagnética de alta frecuencia: la radiación gamma. Lo anterior queda representado por la siguiente ecuación:  Además de núcleos de elementos con átomos más pequeños, se liberan otros neutrones que rompen otros núcleos grandes, en lo que se denomina una reacción en cadena.
Además de núcleos de elementos con átomos más pequeños, se liberan otros neutrones que rompen otros núcleos grandes, en lo que se denomina una reacción en cadena.  La fusión nuclear es un proceso en el que núcleos de átomos muy pequeños se unen para dar núcleos de átomos mayores. Dos átomos de hidrógeno pueden unir sus núcleos y convertirse en un átomo de helio. Este proceso se realiza continuamente en nuestro Sol y en todas las demás estrellas del Universo. Como resultado se desprende una gran cantidad de energía.
La fusión nuclear es un proceso en el que núcleos de átomos muy pequeños se unen para dar núcleos de átomos mayores. Dos átomos de hidrógeno pueden unir sus núcleos y convertirse en un átomo de helio. Este proceso se realiza continuamente en nuestro Sol y en todas las demás estrellas del Universo. Como resultado se desprende una gran cantidad de energía.